蛋白質組學
蛋白質組學(Proteomics)是在1994年由Marc Wikins首先提出的新名詞,蛋白質組被定義為細胞、器官或組織型的蛋白質成分的總稱,而蛋白質組學是研究這些成分在指定的時間或特定的環境條件下的表達。具體來說是對不同時間和空間上發揮功能的特定蛋白質群組進行研究,即在蛋白質水平上探索其作用模式、功能機理、調節調控,以及蛋白質群組內相互作用。其目的是從整體的角度分析細胞內動態變化的蛋白質組成、表達水平與修飾狀態,了解蛋白質之間的相互作用與聯系,揭示蛋白質功能與細胞生命活動規律。因為蛋白質是生理功能的執行者,是生命現象的直接體現者,對蛋白質結構和功能的研究將直接闡明生命在生理或病理條件下的變化機制。
Olink蛋白質組學技術
針對每個待檢蛋白質,Olink設計了一對抗體,抗體上偶聯有特定的DNA單鏈,當這對抗體結合目標蛋白質后,處于鄰位的兩條DNA單鏈可互補結合并經酶延伸形成雙鏈DNA模板,巧妙地將蛋白質定量轉換為DNA定量,最后利用微流控qPCR或NGS測序進行定量檢測。
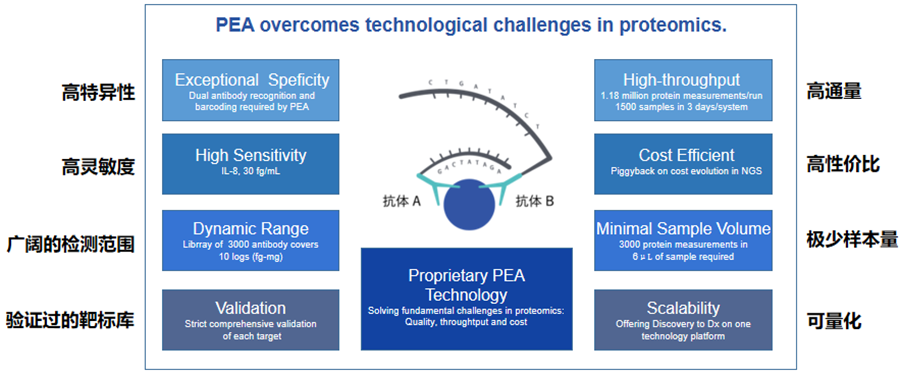
Olink性能特點與技術優勢
在PEA反應中,PCR的指數擴增特性被用來實現對檢測信號對放大,提供較傳統的酶聯免疫吸附試驗(ELISA)更佳的檢測靈敏度。因此只需極小的樣品量就可以同時測量大量的蛋白質,將顯著地促進針對有限及珍貴樣本的研究,例如使用來自臨床隊列或生物樣品庫的人類樣本。此外,PEA中的抗體偶聯的核酸單鏈只有在一一正確配對形成DNA雙鏈時才能被檢測出,這確保了即使在超多重水平下也有超乎尋常的特異性。
性能情況
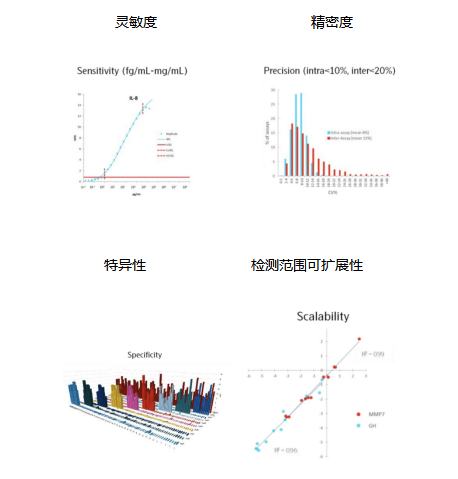
研究流程
Olink技術流程
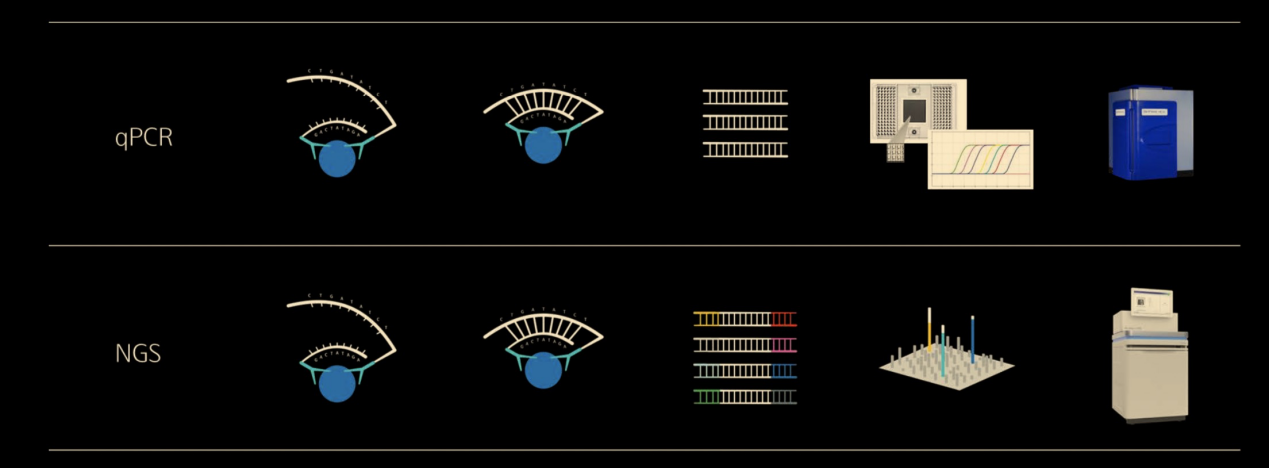
1)樣本孵育后,臨近探針特異性結合目標抗原;
2)探針寡聚體互補并在DNA聚合酶作用下延伸,這將創建一個雙鏈DNA“條形碼”,該條形碼對于特異性抗原來說是唯一的,并且在數量上與靶蛋白質的初始濃度成正比;
3)通過微流控qPCR對擴增子進行定量,或者通過在擴增子上加入接頭進行NGS測序。
Olink生信分析流程與信息分析示例
數據質控
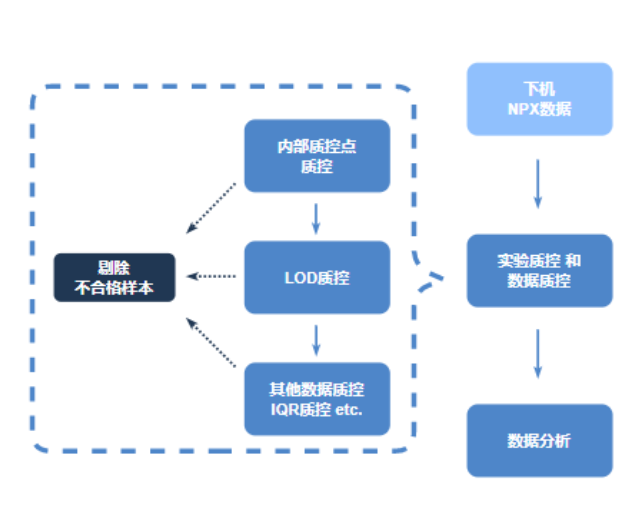
數據分析
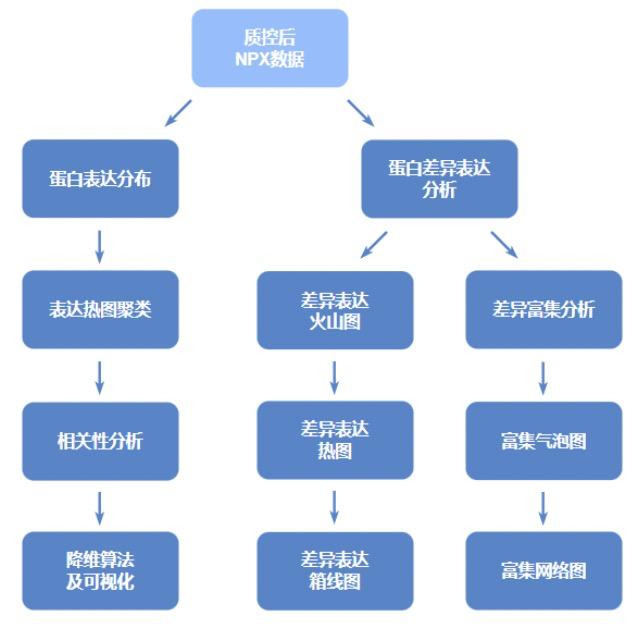
分析結果示意圖
樣本NPX值總覽
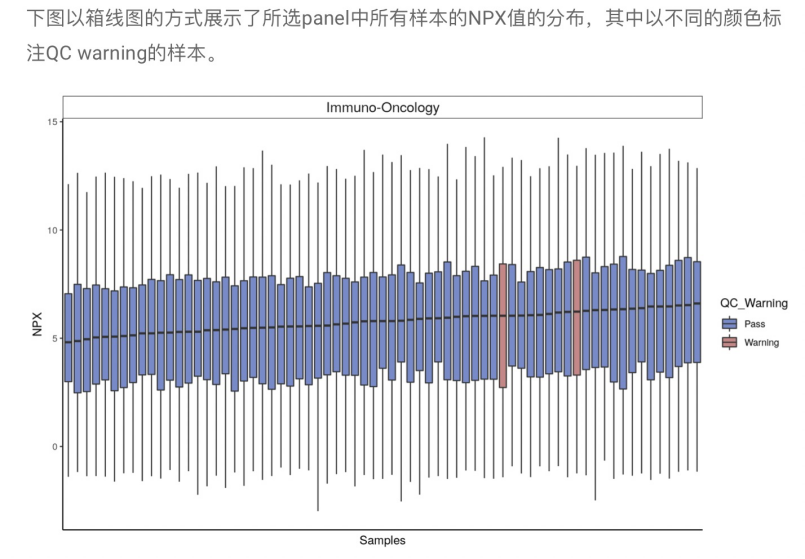
IQR質控

單一分組蛋白表達量熱圖

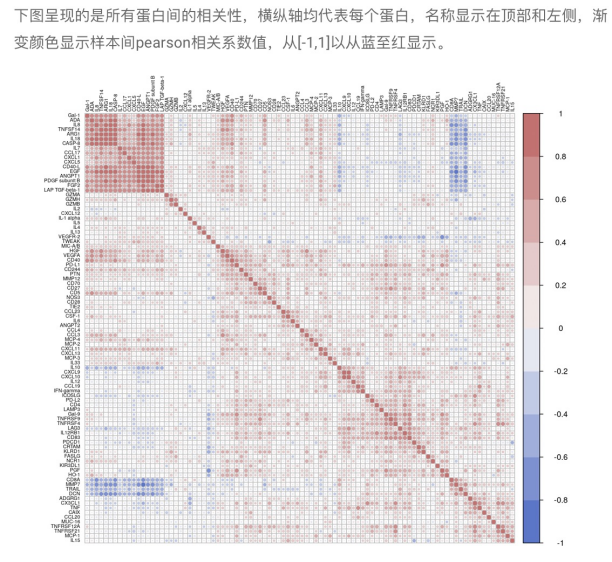
蛋白相關性分析
循環蛋白質組檢測產品
樣本要求
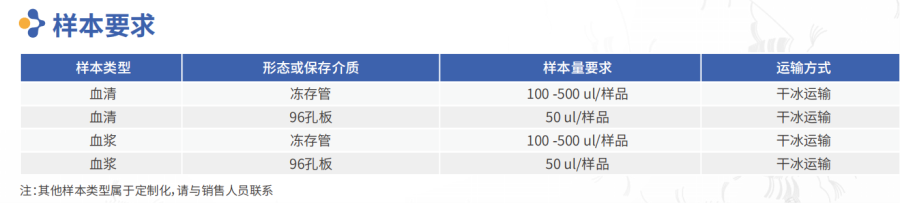
產品服務列表
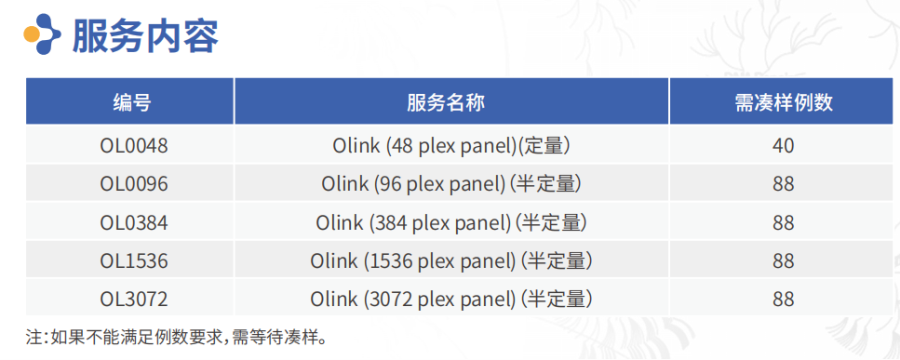
產品服務流程

項目周期
標準流程從樣本接收到數據交付,運轉周期約為 2個月(40 個工作日),選擇定制化信息分析條目需額外評估項目周期。
交付指標和售后服務
1. 根據合同規定完成分析。
2. 提交項目結題報告文檔,說明項目完成情況。
3. 分析過程中產生的項目結題報告、下機原始數據以及相關生物信息分析結果文件。如果數據量小于 100G,使用阿里云提供;因網絡等原因無法順利下載的,可提供移動硬盤傳輸;如果數據量大于 100G,所有數據將會使用移動硬盤傳輸。
4. 數據交付后 6 個月內,提供免費的項目咨詢服務。
5. 最終數據提供后,可繼續保留數據 3 個月,如需延長數據保存時間需做費用評估。
產品服務優勢
Olink的技術優勢總結

案例分析
血漿蛋白質組學助力預測免疫檢查點阻斷劑耐藥的全新生物標志物
研究背景:
免疫檢查點阻斷劑(Immune Check- point Blocker, ICB)現已廣泛應用于腫瘤治療。但很多病人尚未從中獲益,主要歸因于人群的免疫檢查點阻斷劑抵抗。隨著基因組學的快速發展,蛋白質研究已成為深入理解實時生物學的前沿平臺。為解決ICB的潛在毒性,并僅針對可獲益病人進行價格不菲的治療——開發可靠針對ICB抵抗的新型生物標志物,至關重要。
研究思路:
本研究基于Olink技術對兩個獨立接受ICB治療的癌癥患者前瞻性隊列基線血漿樣本(發現隊列n = 95,驗證隊列n = 292)進行了無偏血漿蛋白質組分析。然后,研究者通過Cox比例風險模型研究了血漿蛋白質水平與臨床獲益率、無進展生存期(PFS)、總生存期(OS)以及與PD-L1表達水平、CD8+T細胞浸潤密度、三級淋巴結構TLS的相關性。

研究結論:
血病抑制因子(LIF)可獨立于PD-L1表達狀態預測免疫檢查點阻斷劑治療癌癥患者的效果,且與CD8+T細胞浸潤密度具有相關性。此外,研究者還發現白血病抑制因子(LIF)可獨立于PD-L1表達狀態預測免疫檢查點阻斷劑治療癌癥患者的效果。研究者通過多重免疫組織化學對59例患者的匹配腫瘤組織樣本進行了PD-L1表達評分(下圖a)和CD8+T細胞浸潤密度評估(下圖d),并與LIF水平一起比較臨床結局的相關性。其中,20例患者(33.9%)的PD-L1陽性腫瘤比例評分(TPS)≥1%,39例患者(66.1%)<1%。然而,PD-L1陽性和陰性腫瘤患者的外周LIF水平相似(下圖b),且高水平(46.1%)和低水平循環LIF(55%)的腫瘤患者中PD-L1陽性腫瘤比例相似(數據未顯示)。臨床結局相關性上,無論PD-L1表達狀態如何,具有低水平循環LIF特征的腫瘤患者具有更好的結局。
常見問題 FAQs
? 技術相關
1. Olink的檢測中,每個樣本需要做多少次重復?
Olink對樣本的重復次數沒有要求,除非是客戶要求的。通常來說,生物學重復帶來的變異超過技術變異,所以客戶們更專注于使用不同的樣本而不是做重復實驗。Olink的主要的檢測Panel的板間CV<10%。
2. Olink檢測的靈敏度?
Olink在開發驗證各Panel時,用2倍稀釋的標準曲線去計算了LOD, LLOQ, ULOQ 以及 hook。
已證實:PEA技術的靈敏度高于ELISA檢測,可至fg/ml。Olink使用EDTA 血漿樣本充分驗證了生理病理的蛋白水平。
3. Olink的檢測會受到內源性干擾嗎?預計會有什么基質效應呢?
在進行Olink檢測Panel驗證的時候,Olink評估了來自異嗜性抗體的潛在內源性干擾,例如 人抗鼠抗體 (HAMA) 和類風濕因子,以及特定的干擾物質(溶血物、脂質和膽紅素)。驗證過程中沒有觀察到明顯的測定干擾。
4. 什么是動態檢測范圍(Dynamic Range)?
動態檢測范圍是指介于檢測下限和檢測上限范圍。在這個范圍內,檢測的準確度和精準度更好。
5. 用Olink技術進行的蛋白質組檢測與傳統的DNA測序的主要差別是?
Olink使用NGS(二代測序)作為測量樣本中特定蛋白質生物標志物的相對濃度。在樣本和文庫制備過程中,會產生對標每個蛋白質生物標志物的特定序列(DNA條形碼)的短DNA鏈。測序后,這些特定序列的DNA鏈的技術與原始蛋白質生物標志物的濃度成正比。
? 產線相關
1. 在Olink的每個檢測試劑盒中可以檢測到多少種蛋白質生物標志物?
對于Olink的Target系列而言,除了可以檢測到的內部參照, Target 96 和Target 48可以分別實現92個/45個不同靶標蛋白的檢測。
2. 從哪里可以獲取關于Olink檢測Panel中的某個特定蛋白質的更多的信息?
可以通過訪問一些公開公共的資源,例如Human Protein Atlas網站、UniProt數據庫等。
3. 一個Olink Explore系列的試劑盒可以檢測多少蛋白質生物標志物?
除去對照, 一個Explore 384 試劑盒包含了368種蛋白質生物學標志物,而一個 Explore 3072的試劑盒,包含了8個 Explore 384的檢測Panel,總共可以平行檢測2944個蛋白質。
4. 在不同的Explore 384 Panel中,是否有重疊的檢測?為什么?
不同的Explore 384 Panel中都有IL6, IL8和TNF-?± 檢測。它們用作額外的對照步驟。
5. 定制的Focus Panel可檢測的靶標數目的上限和下限是多少?
目前,Olink Focus Panel可檢測的靶標數目的上限是21、下限是1。但開發靶標上限和下限的檢測Panel的價格是一樣的。
6. Focus Panel中的靶標蛋白可以不是Olink靶標庫中的嗎?
不行,僅有Olink靶標庫中的蛋白質可做Focus Panel。
7. Olink Panel中的靶標蛋白是如何選擇的呢?
在設計新的Panel時,Olink從廣泛使用的公共訪問生物信息學數據庫中收集信息,包括 UniProt、Human Protein Atlas、Gene Ontology (GO) 和 DisGeNET。
先選擇已知和探索性生物標志物的組合并評估合適抗體的可用性,然后還需要通過Olink嚴格的驗證測試和要求。 選擇過程和Panel組成是根據各個領域專家的意見共同制定的。
8. Olink的Panel中用的是什么抗體?
Olink各檢測Panel用的都是抗原純化的多克隆或單克隆抗體或者是兩者的組合。絕大部分都是商業化的抗體。
? 樣本相關
1. Explore和Target系列可接受的樣本類型有哪些?
對于Explore系列,Olink在人類血漿血清樣本上進行了充分地驗證。
對于其他類型的樣本,例如組織和細胞裂解物、細針活檢、外泌體、微透析液、支氣管肺泡灌洗液、細胞培養基、干血斑、滑液、腦脊液、斑塊提取物、尿液、唾液等等 ,需在實驗室內進行驗證后再進行檢測。
2. 收樣體積
雖然Explore 384僅需1μL/樣本、Explore 1536需要 4μL/樣本用于檢測,但由于使用各類移液設備,需要考慮到額外的死腔體積,因此我們要求每個96孔板中最少要保留10μL/樣本。
考慮到運輸過程中可能會伴有液體蒸發等,我們要求運輸時,最低樣本體積為50μL/樣本。如有必要,我們可以返還剩余樣本給您。
? 服務相關
1. 各Olink panels中需要提供的樣本數目是多少?
對于Olink Explore系列產品和Olink Target 96 產品, 針對一塊96孔板,需要湊齊88個樣本。對于Olink Target 48 產品, 針對一塊48孔板,需要湊齊40個樣本。
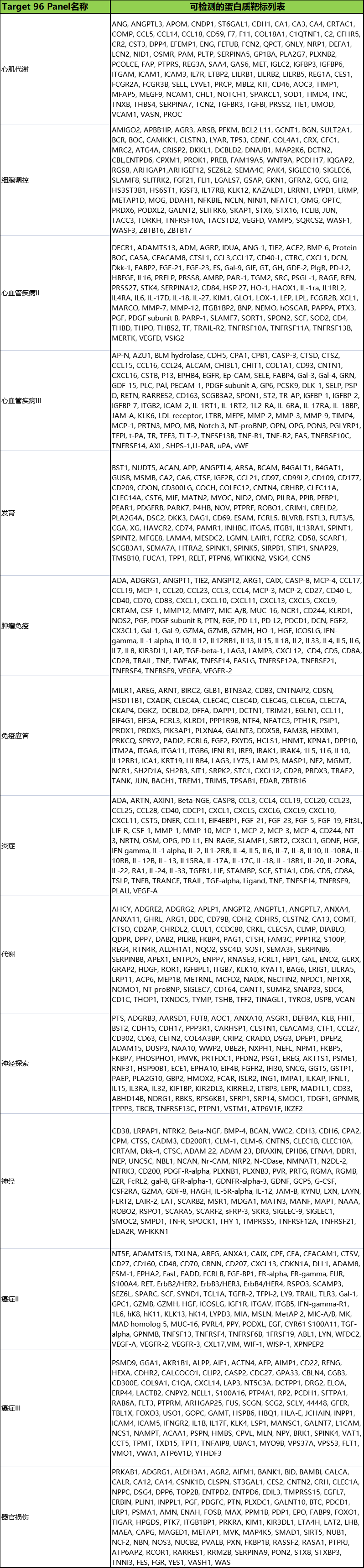
附錄:Olink-Target 96-系列Pane的檢測靶標列表
Copyright?2021
深圳裕策生物科技有限公司 版權所有
粵ICP備16128839號

